Der forensische Kampf gegen Arzneimittelfälschungen
Der forensische Kampf gegen Arzneimittelfälschungen
Bessere Bestimmung illegaler PDE-5-Inhibitoren mithilfe von UHPLC-MS/MS





Phosphodiesterase (PDE)-5-Hemmer wie Viagra® sind für die Behandlung von erektiler Dysfunktion (ED) zugelassen und werden häufig eingesetzt. Allerdings sind auch einige nicht zugelassene, synthetische PDE-5-Inhibitoren leicht erhältlich, insbesondere auf Online-Marktplätzen. Viele dieser Substanzen sind gefährlich und haben in der Vergangenheit bereits gesundheitliche Schäden verursacht oder sogar zu Todesfällen geführt. Die erfolgreiche strafrechtliche Verfolgung der Anbieter dieser Produkte ist maßgeblich von der forensischen Toxikologie abhängig. Wissenschaftler in Polen haben nun eine Methode entwickelt, um den Nachweis illegaler PDE-5-Substanzen mithilfe von UHPLC-MS/MS-Ausrüstung von Shimadzu zu vereinfachen.
Illegale Nachahmer als Trittbrettfahrer
Medikamente zur Behandlung von erektiler Dysfunktion (ED) erfreuen sich großer Beliebtheit und sind extrem lukrativ. Dadurch kommt es zu einer zunehmenden Anzahl an Fälschungen und anderen nicht zugelassenen Medikamenten, die dieselben Ergebnisse versprechen wie geprüfte und zugelassene Medikamente, zum Beispiel Viagra®.
Viele dieser sogenannten Medikamente sind nicht nur illegal, sondern können für Menschen gefährlich – und sogar tödlich sein.
Das Problem der erektilen Dysfunktion
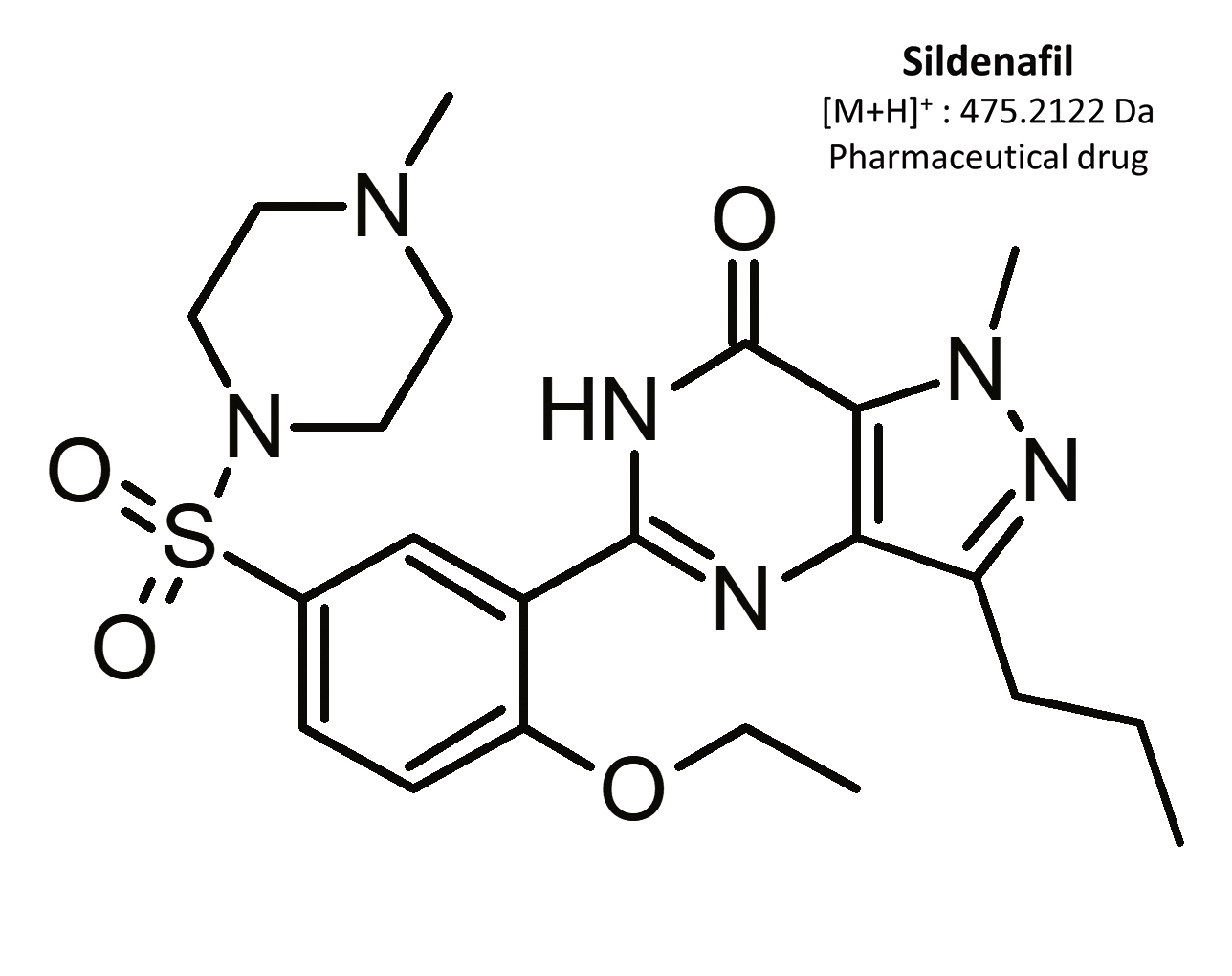
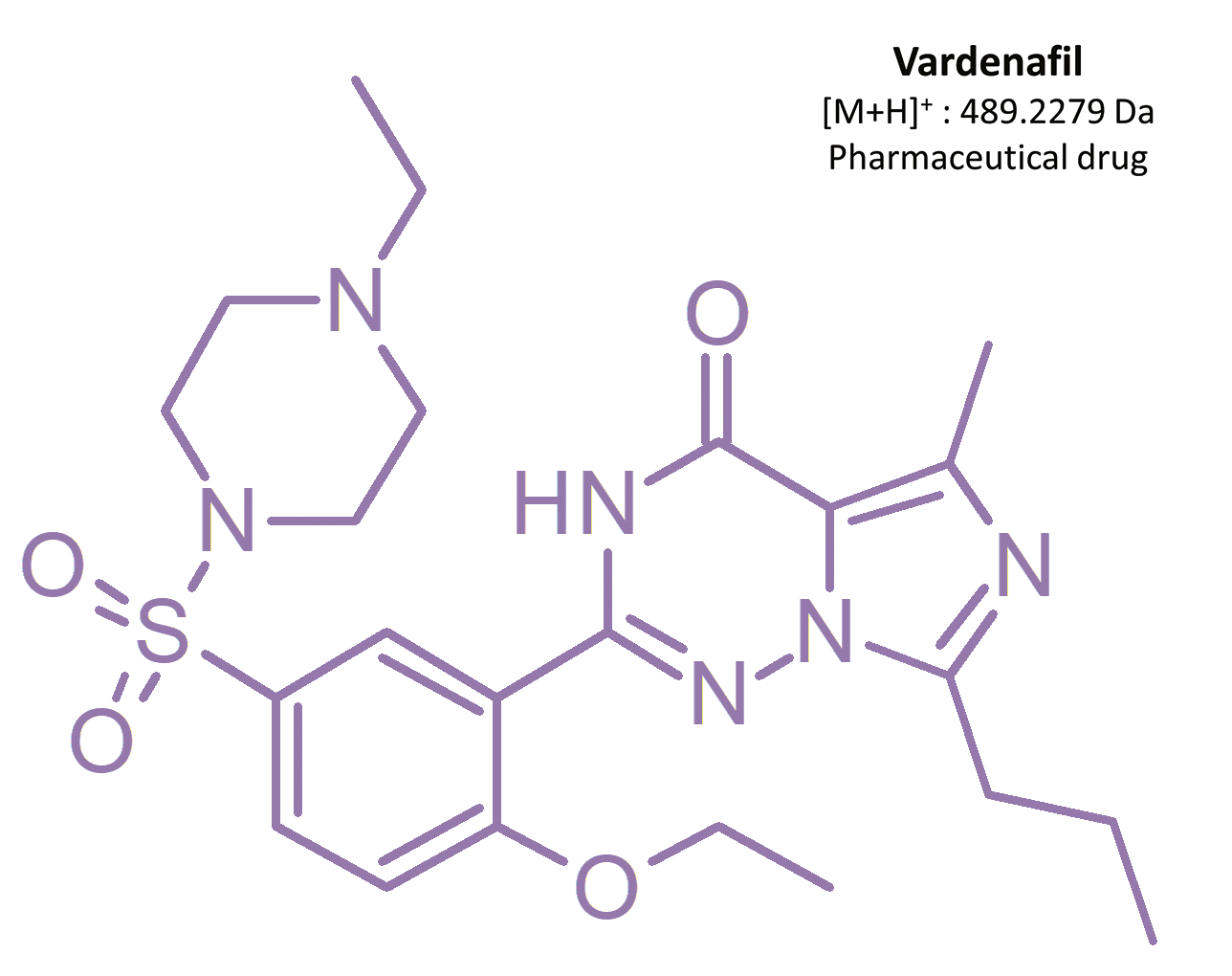
ED beschreibt das dauerhafte Unvermögen, eine Erektion zu erreichen und/oder aufrechtzuerhalten, wodurch der Geschlechtsverkehr eingeschränkt wird [1]. Schätzungen zufolge sind weltweit über 150 Millionen Männer von dieser Krankheit betroffen [2]. In Polen leiden 1,5 Millionen Männer an ED; 60 % davon sind zwischen 40 und 60 Jahre alt [3]. Die Erstlinientherapie bei ED sieht oral einzunehmende Medikamente vor, die selektive und reversible Phosphodiesterase (PDE)-5-Inhibitoren enthalten. Dieses Enzym kommt vorrangig im Corpus cavernosum penis, also dem Schwellkörper des Penis, sowie im Lungenkreislauf vor [3, 4, 5]. Die am häufigsten eingesetzten Arzneimittel sind Sildenafil und das Analogon Vardenafil.
Sildenafil war der erste orale PDE-5-Inhibitor, der für die Behandlung von ED zugelassen wurde. Im Jahr 1996 erhielt Pfizer Inc. von der US-amerikanischen Arzneimittelbehörde FDA die Zulassung dafür, Sildenafil unter der Handelsbezeichnung Viagra® herzustellen [16]. Das Produkt kam 1998 auf den Markt und erzielte in den ersten drei Monaten einen Umsatz von 411 Millionen US-Dollar [17]. Sildenafil erfreute sich sehr schnell großer Beliebtheit und wurde in den ersten sechs Monaten nach der Markteinführung sechs Millionen Mal verschrieben [18]. Schätzungen zufolge stellten mehr als 700.000 Ärzte in den ersten sieben Jahren, nachdem Sildenafil auf den Markt gekommen war, über 150 Millionen Rezepte für nahezu 27 Millionen Männer aus. Sildenafil ist mittlerweile ein in weltweit über 120 Ländern zugelassenes Arzneimittel [2].
2003 kam Vardenafil als alternative ED-Behandlung auf den Markt [6]. Sowohl Sildenafil als auch Vardenafil weisen einen vergleichbaren Wirkmechanismus, eine ähnliche Wirksamkeit und vergleichbare Behandlungsindikationen auf. Außerdem wurden weitere Medikamente zur Behandlung von erektiler Dysfunktion eingeführt, die andere Phosphodiesterase-5-Inhibitoren enthalten, unter anderem Tadalafil und Avanafil [19].
Der Erektionsmechanismus
Bei sexueller Erregung wird im Schwellkörper des Penis Stickstoffmonoxid (NO) freigesetzt, wodurch die Guanylatcyclase aktiviert wird und der cGMP-Spiegel (cyklisches Guanosinmonophosphat) steigt. In Folge kommt es zur Kontraktion der glatten Muskeln im Schwellkörper, hauptsächlich unter der Beteiligung von PDE-5. Kommt es zu einer Hemmung der PDE-5-Aktivität, wird ein Anstieg der cGMP-Konzentration beobachtet. Dies führt zu einer Kontraktion der glatten Muskeln im Schwellkörper, zu einem Anstieg des Blutflusses in den Schwellkörper und damit zu einer Erektion [3, 4, 7].
Sildenafil wird im Übrigen nicht nur zur Behandlung von ED eingesetzt, sondern auch bei Lungenhochdruck und zur Vorbeugung der Höhenkrankheit (akutes Höhenlungenödem), z. B. Revatio®. Sildenafil erhöht die cGMP-Konzentration in den glatten Muskelzellen der Lungengefäße und führt zur Diastole. Bei Menschen, die an Lungenhochdruck leiden, lässt sich eine pulmonale Vasodilatation (Erweiterung der Blutgefäße in der Lunge) beobachten, wobei die Vasodilatation im normalen Blutkreislauf gering bleibt [8].
Pharmakokinetik von PDE-5-Inhibitoren
Sildenafil und andere zugelassene PDE-5-Inhibitoren sind als Tabletten mit Filmüberzug, als Tabletten, die sich in der Mundhöhle auflösen, als Kautabletten und in Pulverform zur Herstellung einer oralen Suspension erhältlich. Zur Behandlung von ED ist Sildenafil in Dosierungen von 25 mg, 50 mg und 100 mg erhältlich. Es wird empfohlen, die Behandlung mit einer Dosis von 50 mg zu beginnen und danach die Therapie den Ergebnissen entsprechend anzupassen [9].
Sildenafil wird nach oraler Verabreichung schnell resorbiert, und die maximale Konzentration im Plasma wird nach 30 bis 120 Minuten erreicht [10, 11], im Durchschnitt nach 60 Minuten [1]. Die Zeit, die durchschnittlich benötigt wird, um eine Erektion zu erreichen, beträgt etwa 30 Minuten, und die Wirkungsdauer des Arzneimittels beträgt etwa 4 bis 5 Stunden [9].
Nach der oralen Verabreichung liegt die Bioverfügbarkeit bei 38 bis 41 % [12, 13]. Der Verzehr einer fettreichen Mahlzeit führt zu einem Rückgang der Medikamentenkonzentration im Plasma um 29 % und verlängert die Zeit, die erforderlich ist, um eine maximale Konzentration im Plasma zu erreichen, um eine Stunde [6]. Eine orale Einmalgabe (25 mg) bei 12 Patienten führte zu einer durchschnittlichen maximalen Plasmakonzentration von 159 ng/ml nach 0,5 bis 2,5 Stunden. Die biologische Halbwertszeit von Sildenafil liegt bei 3,2 Stunden [7] bis 4,1 Stunden [1].
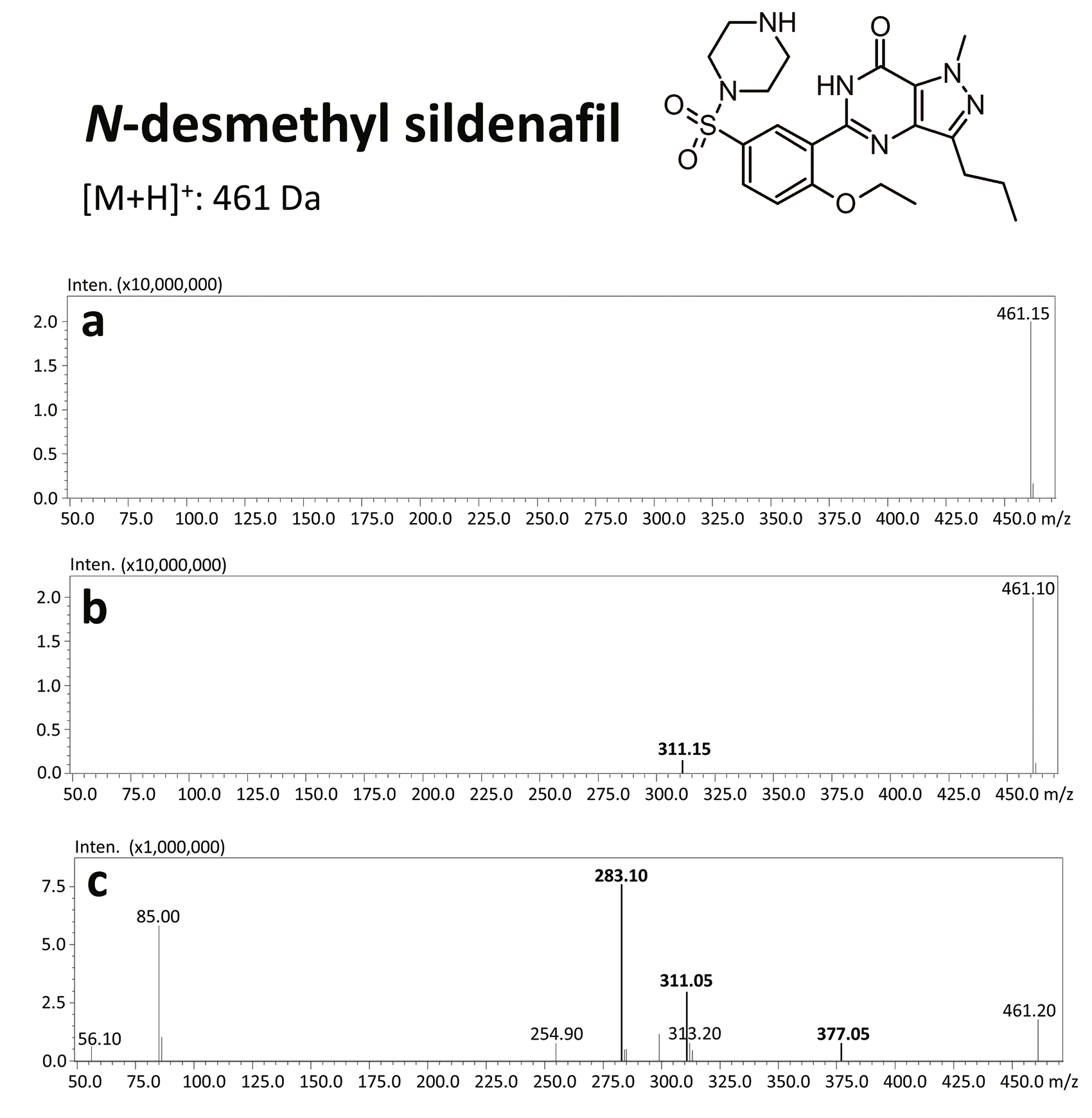
Sildenafil wird in der Leber mithilfe der Cytochrome P450, insbesondere CYP3A4 und, in geringerem Maße, CYP2C9, durch N-Demethylierung metabolisiert [14]. Infolgedessen wird ein Hauptmetabolit von Sildenafil gebildet – N-Desmethylsildenafil – der 45 bis 50 % der Aktivität von Sildenafil aufweist [1, 15]. Sildenafil wird primär über Stuhl (80 %) und sekundär (13 %) über Urin ausgeschieden [7].
Nicht zugelassene ED-Medikamente – ein gefährlicher Markt
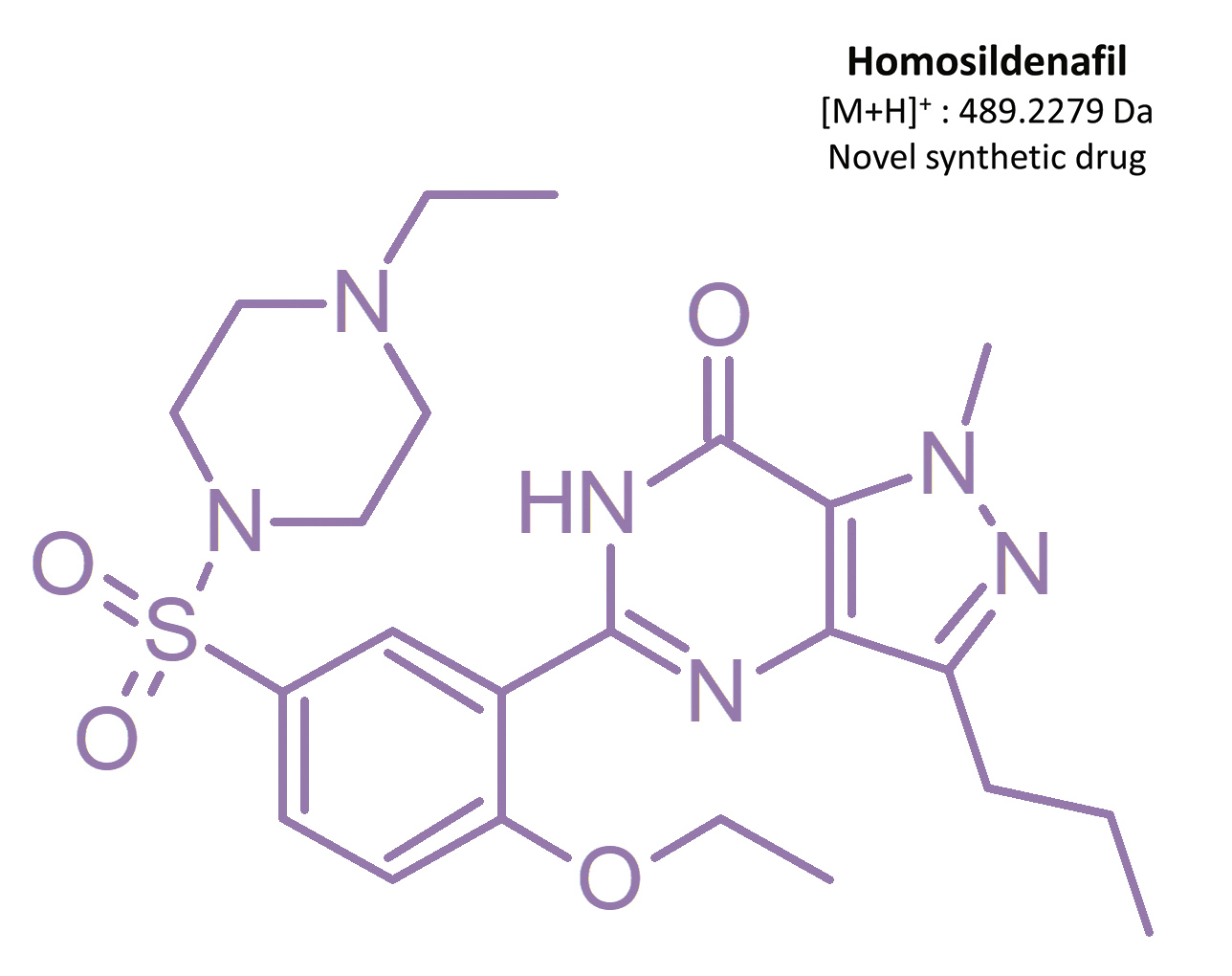
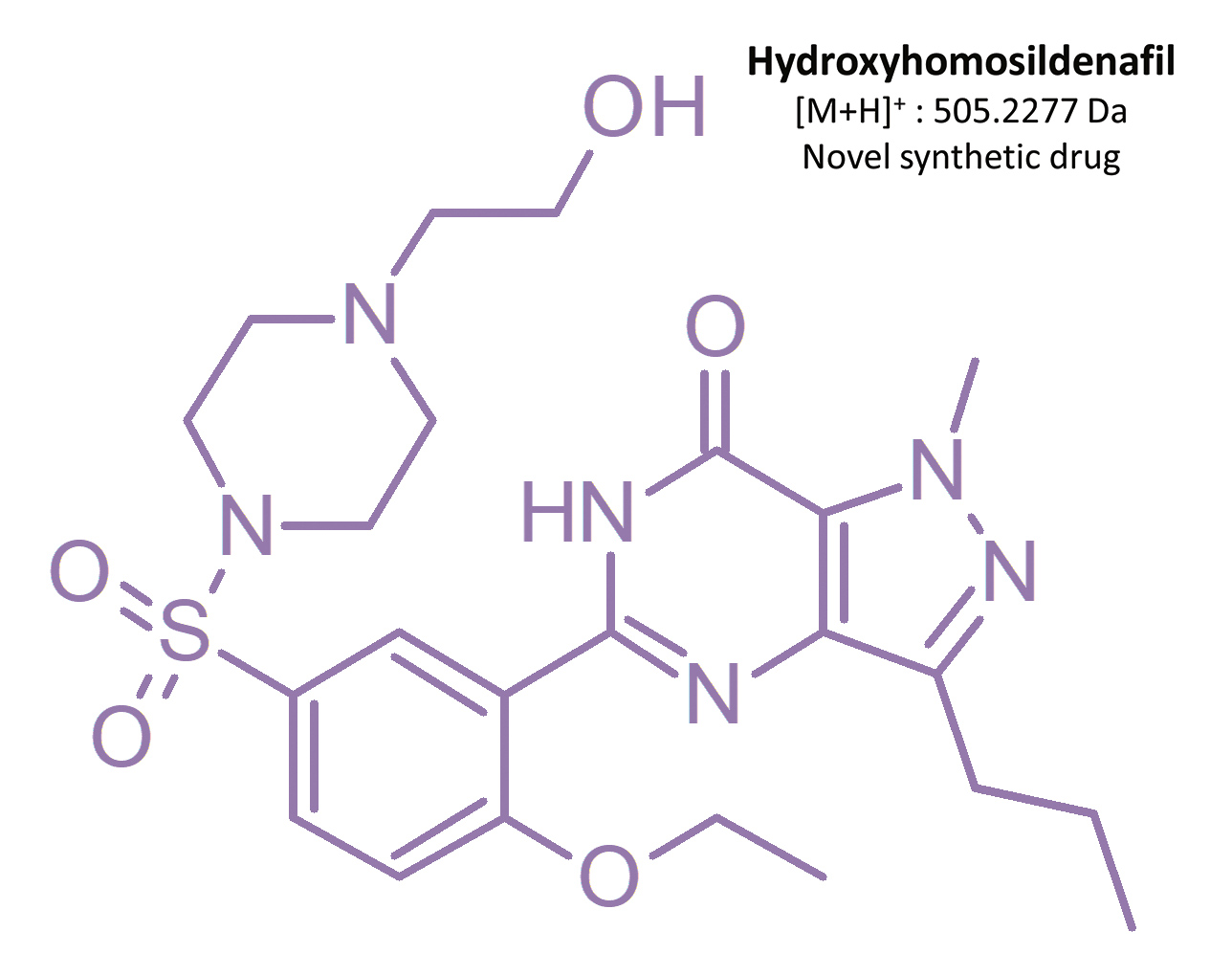
Bereits vor dem Patentablauf von Viagra® im Jahr 2013 [19] erschienen Konkurrenzprodukte auf dem Markt, die weder für die medizinische Anwendung zugelassen noch auf ihre Verbrauchersicherheit hin untersucht worden waren – darunter auch synthetische Analoga von Sildenafil. Im Zeitraum von 2002 bis 2014 wurden 39 illegale Wirkstoffe entdeckt [16], am häufigsten: Homosildenafil; Hydroxyhomosildenafil; Hongdenafil; Hydroxyhongdenafil; Aminotadalafil; Piperidenafil und Methiosildenafil [20].
Diese Wirkstoffe können in pflanzlichen Nahrungsergänzungsmitteln, Arzneimitteln unbekannter Herkunft und Pulvern in Großpackungen gefunden werden [20, 21]. Zum Beispiel wurden Homosildenafil und Hydroxyhomosildenafil in pflanzlichen Tabletten gegen Müdigkeit nachgewiesen, die als „pflanzliches Viagra“ verkauft werden [22]. Zou et al. [17] fanden Sildenafil, Homosildenafil, Hydroxyhomosildenafil, Hongdenafil, Vardenafil und Tadalafil in Pulverproben aus Großpackungen, während Do et al. Tadalafil und Sildenafil in 31 kommerziellen Produkten nachweisen konnten [23]. Ein weiteres Sildenafil-Analogon – Isosildenafil – wurde bisher wenig untersucht und ist nicht für die medizinische Anwendung zugelassen [19].
Tatsache ist, dass gefälschte und andere illegale Substanzen, die als seriöse, zugelassene Medikamente angepriesen werden, ein erhebliches Gesundheitsrisiko darstellen. Glibenclamid, Talkumpuder, Amphetamine und Farbstoffe sind nur ein Teil der Unreinheiten, die in illegalen ED-Medikamenten gefunden wurden. Der Gebrauch von sowohl illegalen als auch pharmazeutischen PDE-5-Inhibitoren kann zu Kopfschmerzen, Muskelschmerzen, Übelkeit, Erbrechen, Hitzewallungen und Sehstörungen führen. Und im Falle nicht zugelassener Konzentrationen können Bluthochdruck und ähnliche Nebenwirkungen auftreten. Besonders gefährlich ist dies, wenn die Einnahme zusammen mit anderen gefäßerweiternden Mitteln wie Alkylnitriten, auch bekannt als „Poppers“, erfolgt. Im schlimmsten Fall kann dies sogar zum Tod führen.

Einsatz von UHPLC-MS/MS bei der forensischen Ermittlung von gefälschten Arzneimitteln
Im Rahmen eines Gerichtsverfahrens, bei der es um eine Vergiftung mit Todesfolge ging, bat die zuständige Strafverfolgungsbehörde das Institute of Toxicology Research in Borowa, Polen, um Unterstützung bei der toxikologischen Analyse eines mutmaßlich gefälschten Präparats. Die Wissenschaftler des Instituts kamen der Bitte nach und entwickelten dabei eine nützliche neue Methode, die der Ermittlung illegaler ED-Medikamente dient.
Dazu hatte das Institut zuvor eine Screening-Methode für die zeitgleiche Bestimmung vieler Wirkstoffgruppen entwickelt, darunter auch PDE-5-Inhibitoren und ihre Metaboliten. Diese Methode wurde durch Verwendung von dotierten Blutproben und einer Quantifizierungsmethode unter Verwendung eines internen Standards entwickelt und umfassend validiert.
Bei dieser Methode basiert das Probenvorbereitungsverfahren auf einer schnellen und einfachen Flüssig-Flüssig-Extraktion (pH 9 mit Ethylacetat). Die Ermittlung unbekannter Substanzen gelang durch den Einsatz eines Shimadzu Nexera X2 Ultra-Hochleistungsflüssigkeitschromatographen (Ultra-High-Performance Liquid Chromatograph, UHPLC) in Kombination mit einem Shimadzu LCMS-8050 (QqQ) Tandem-Massenspektrometer.
Aufgrund der hohen Empfindlichkeit dieser Geräte konnte das Probenvolumen auf nur 200 µl reduziert werden. Für die Screening-Analyse der vom Gericht zur Verfügung gestellten Blutprobe wurde der Q3-Scan-Modus verwendet, während die Bestimmung der chemischen Verbindungen mittels Produktionen-Scan-Experimenten erfolgte. Vorläufer-Ionen wurden bei drei Kollisionsenergien fragmentiert (10, 20 und 35 V).
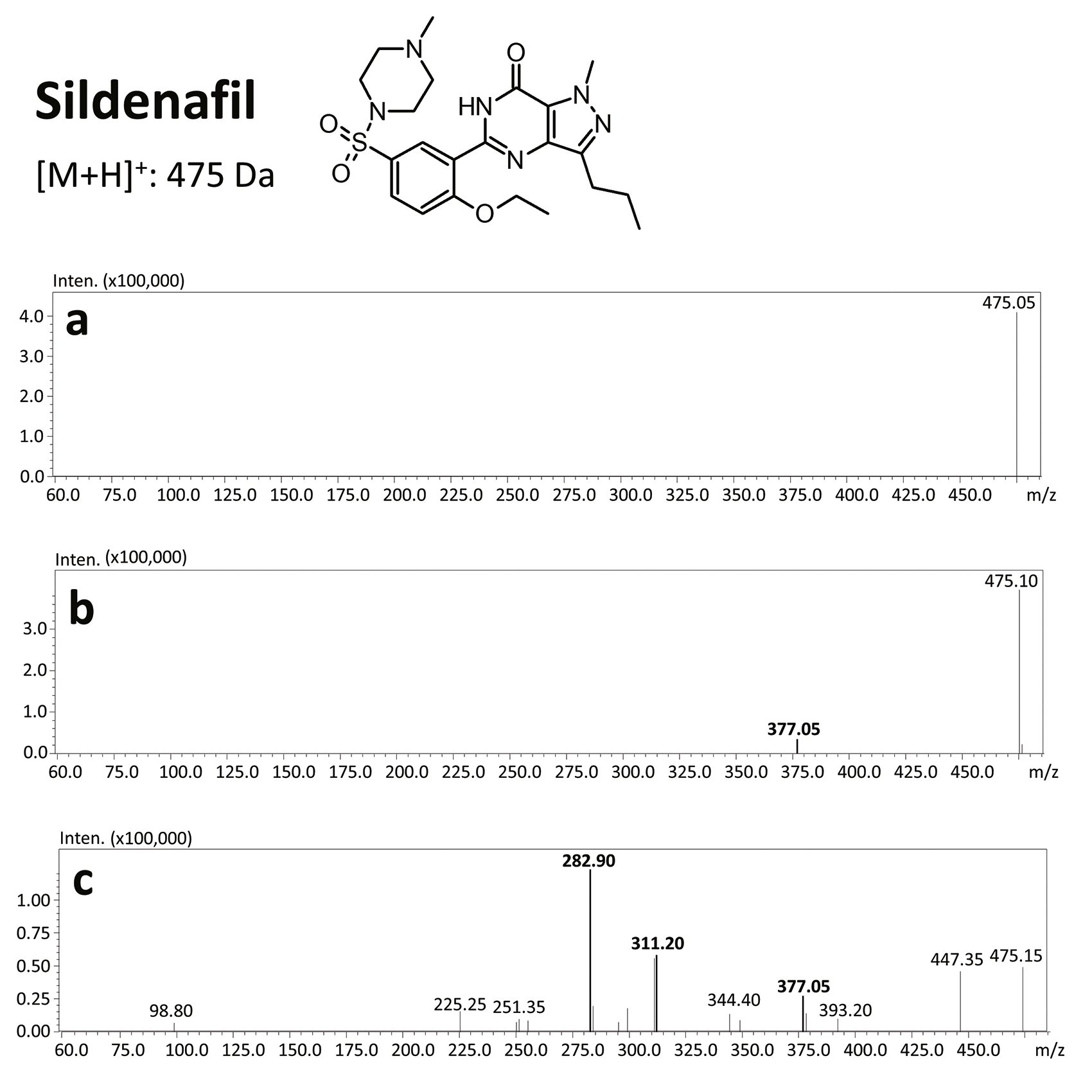
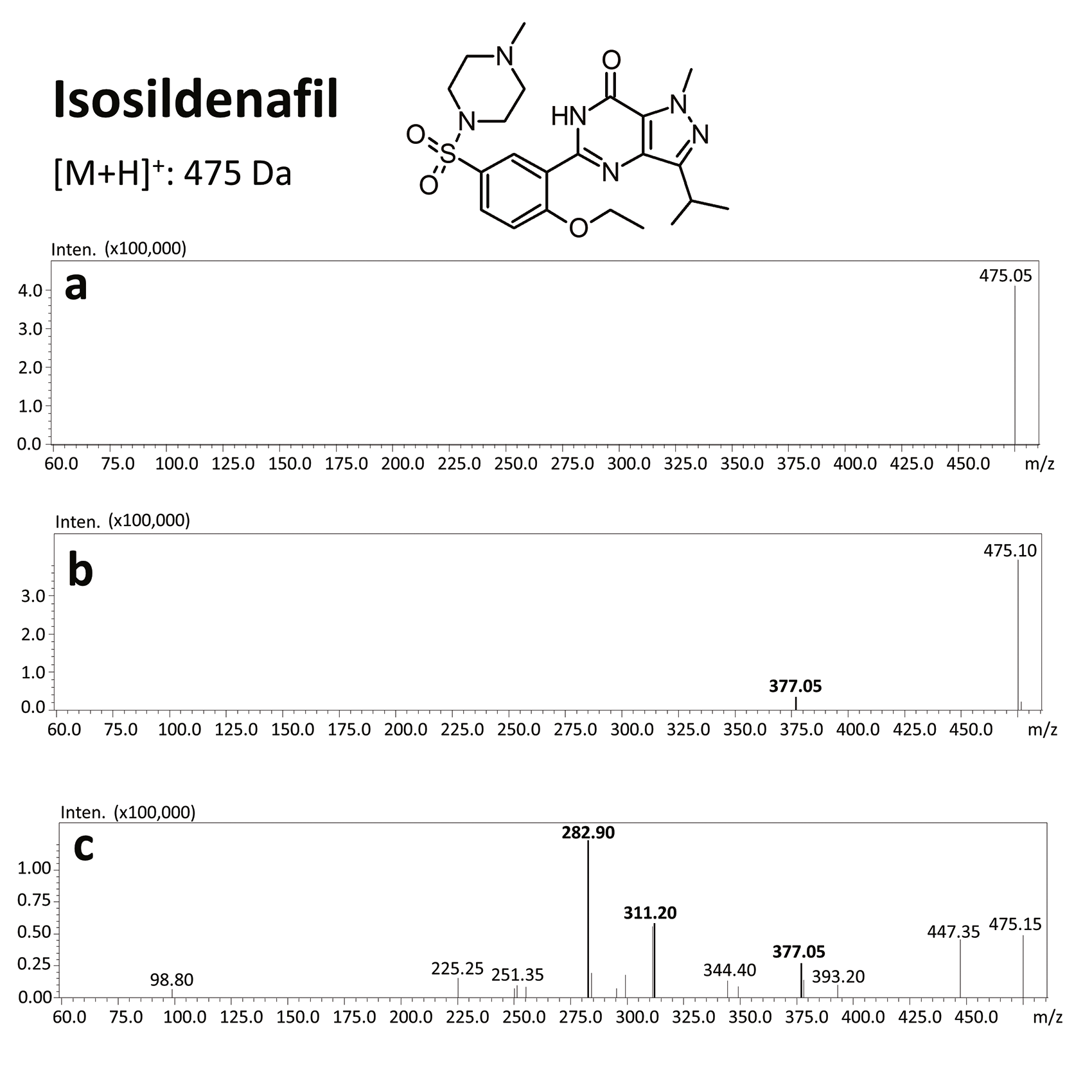
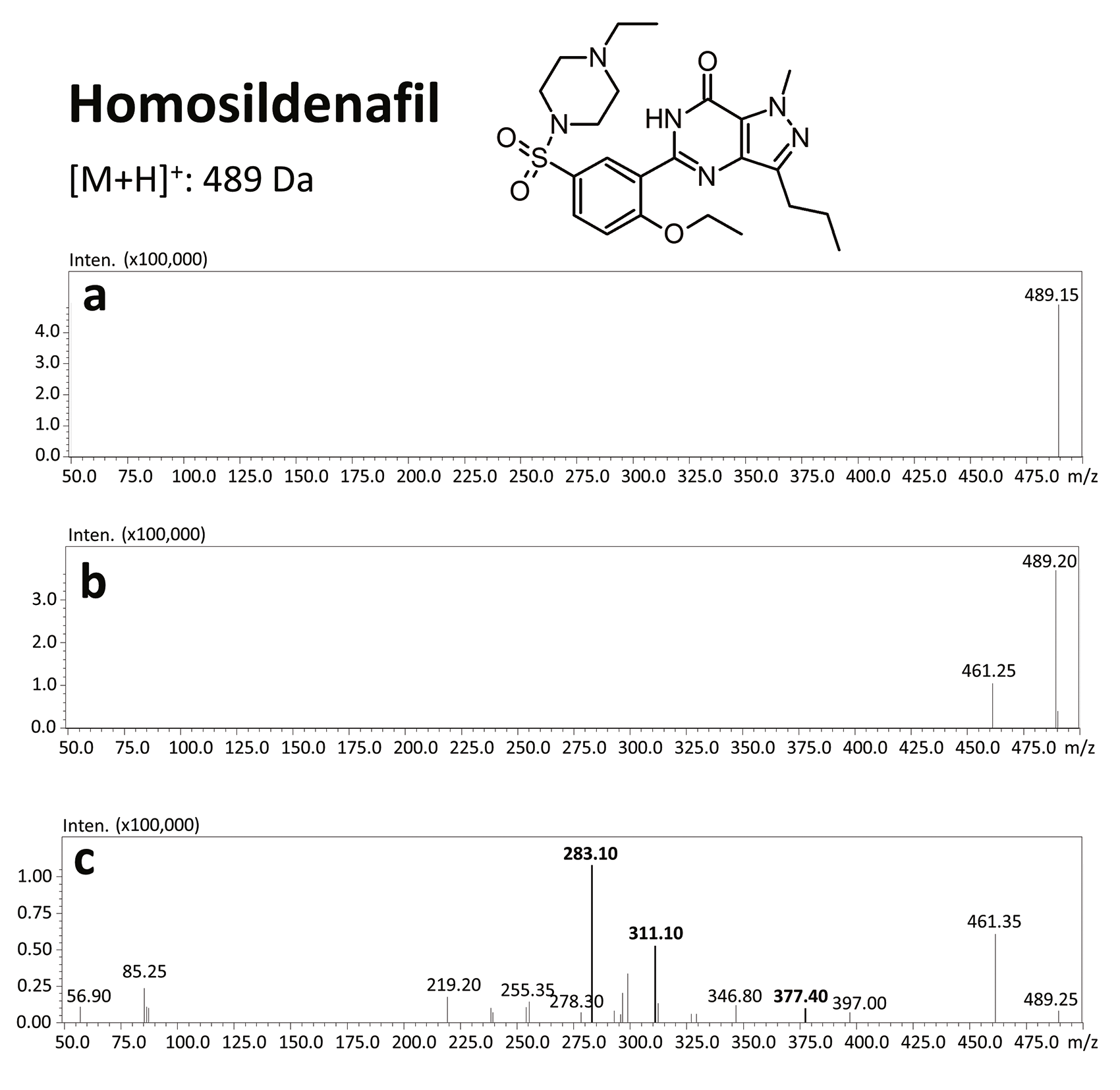
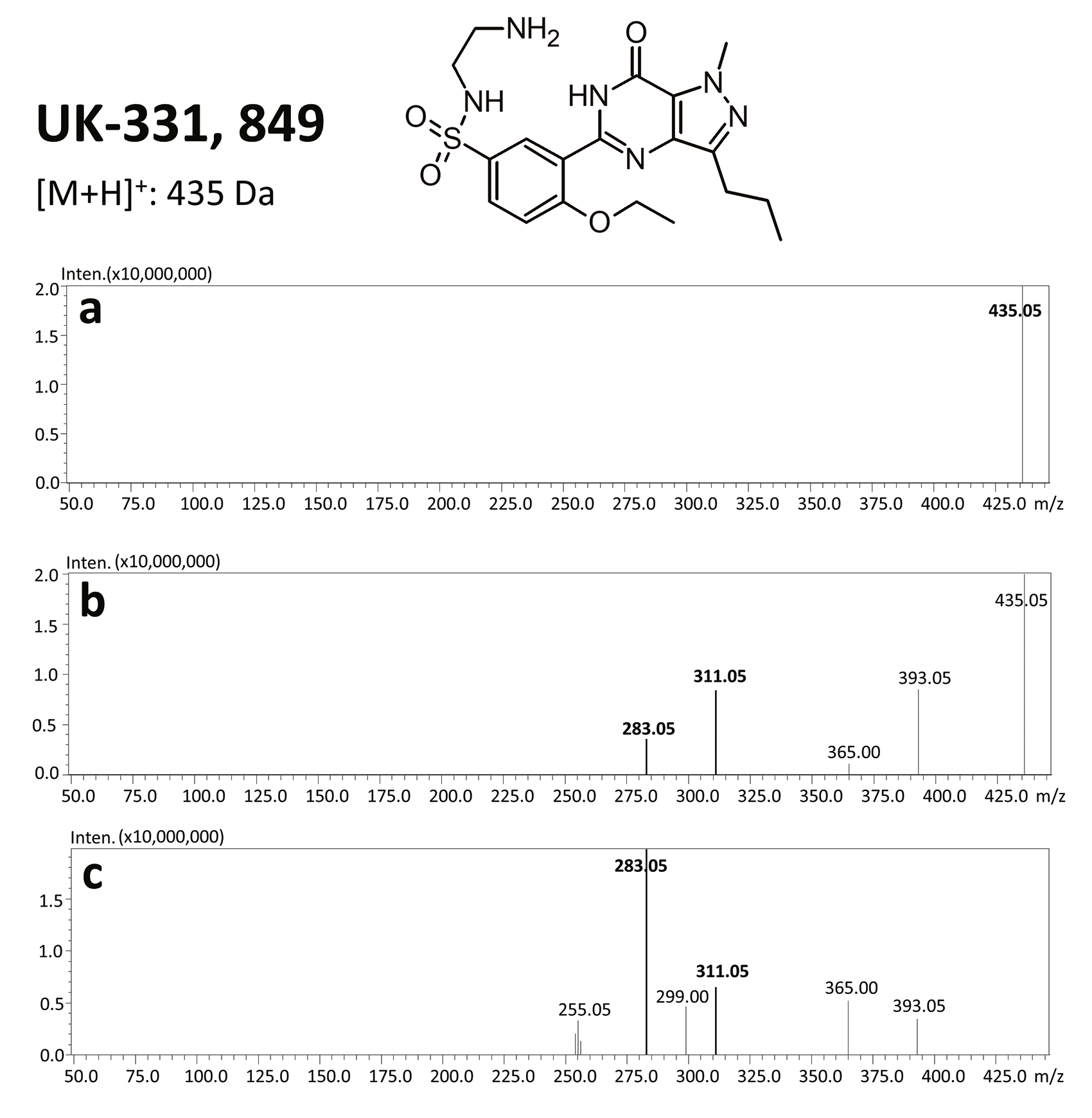
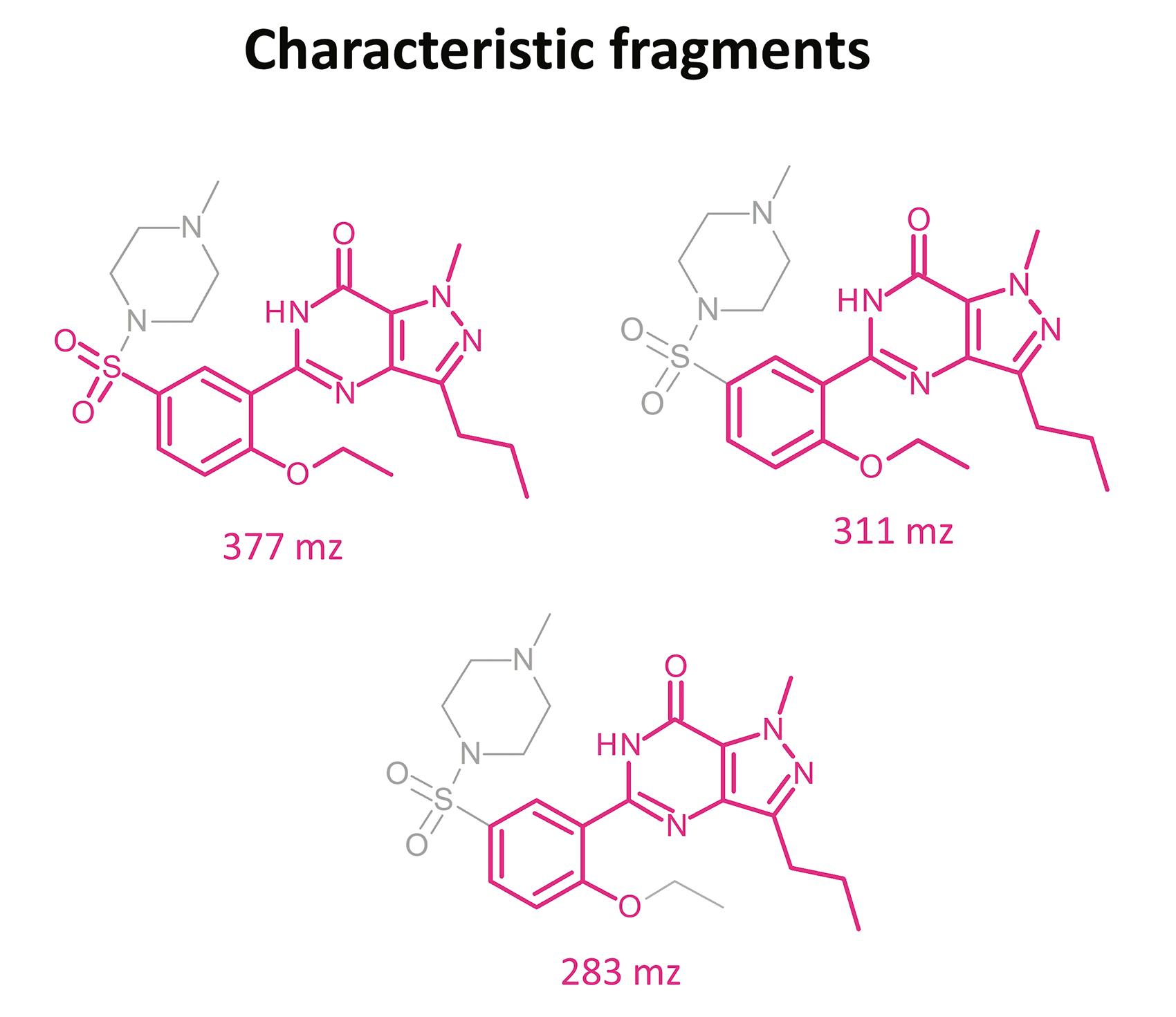
Die Ergebnisse dieser toxikologischen Analyse mit detaillierten chromatographischen und massenspektrometrischen Bedingungen sowie charakteristischen Fragmenten sind in den Abbildungen dargestellt. Fünf Analoga, die zur Gruppe der Phosphodiesterase-Inhibitoren gehören, darunter zwei Metaboliten, wurden mithilfe der oben genannten Methode identifiziert. Bei den nachgewiesenen Substanzen handelte es sich um Sildenafil und seine Metaboliten (N-Desmethylsildenafil und UK-331, 849) sowie um zwei synthetische Analoga von PDE-5-Inhibitoren (Isosildenafil und Homosildenafil), deren Vorhandensein im Blut darauf hindeuten kann, dass das Medikament von illegalen Akteuren hergestellt und/oder erworben wurde.
Die Gefahr, die mit Sildenafil-Analoga einhergeht, begründet sich im Mangel an Daten bezüglich Toxizität und Sicherheit. Da ihre Struktur der von legalen Phosphodiesterase-5-Inhibitoren wie Sildenafil ähnelt, können die Analoga tatsächlich auch ähnlich wirken. Andererseits weisen sie möglicherweise eine höhere oder geringere Wirksamkeit auf – die auf die Einnahme folgende Reaktion ist daher gänzlich unvorhersehbar. Durch diese mangelnde Vorhersehbarkeit und die Tatsache, dass Sildenafil, andere Phosphodiesterase-5-Inhibitoren und ihre Analoga in einer Reihe von weithin erhältlichen Produkten enthalten sein können, entsteht ein großer Bedarf an schnellen, einfachen und zuverlässigen Methoden zur Substanzermittlung.
 Fazit
Fazit
Durch die Adaption einer zuvor entwickelten Methode für biologische Analysen konnten die Wissenschaftler das Vorhandensein gefährlicher Substanzen – PDE-5-Analoga und deren Metaboliten – in nicht zugelassenen Medikamenten zur Behandlung von ED identifizieren und quantifizieren.
Die von ihnen entwickelte Methode bietet einen soliden reproduzierbaren Ansatz, der für Toxikologen und klinische oder analytische Chemiker von Interesse ist, die versuchen, neue, auf dem illegalen Arzneimittelmarkt auftauchende Substanzen aufzuspüren und nachzuweisen. Anhand dieser Methode wird die hohe Empfindlichkeit und Selektivität des Shimadzu Nexera X2 sowie die Tatsache sichtbar, dass Q1/Q3 dank seiner Hochgeschwindigkeits-MS/MS-Detektion in einem Scanning-Modus verwendet werden kann. Dies ist für diese Art von Detektor einzigartig. Darüber hinaus minimiert die Methode den Einsatz von biologischem Probenmaterial, so dass bei der Probenvorbereitung wesentlich geringere Mengen an organischen Lösungsmitteln benötigt werden.
Chromatographische und massenspektrometrische Bedingungen
Die Analysen wurden mit einem UHPLC-System, dem Shimadzu Nexera X2 (Kyoto, Japan), durchgeführt. Die Trennung erfolgte mit einer Kinetex XB-C18-Säule (150 x 2,1 mm Innendurchmesser, Partikelgröße 2,6 µm; Phenomenex, Torrance, CA, USA bei einer Säulentemperatur von 40 °C. Die mobile Phase bestand aus 0,1 % Ameisensäure in Wasser (A) und 0,1 % Ameisensäure in Acetonitril (B). Die Gradientenelution wurde mit einem konstanten Fluss von 0,4 ml/min durchgeführt. Folgender Gradient wurde verwendet: 0 min, 5 % B; 12 min, 98 % B; 14 min, 98 % B und 15 min, 5 % B. Die Rückkehr zur ursprünglichen Gradientenzusammensetzung (95 % A/5 % B) wurde 5 Minuten lang durchgeführt.
Der Nachweis der untersuchten Verbindungen wurde mit einem QqQ-MS/MS, Shimadzu LCMS-8050 (Kyoto, Japan), erbracht. Das Spektrometer war mit einer Elektrospray-Ionisationsquelle (ESI) ausgestattet; die Ermittlung der untersuchten Substanzen erfolgte im Produkt-Ionen-Scan-Modus. Die folgenden MS-Parameter wurden festgelegt: Nebulizing Gas, 3 l/min; Heating Gas, 10 l/min; Interface-Temperatur, 250 °C; Desolvation Line Temperatur, 200 °C; Heizblocktemperatur, 350 °C und Drying Gas, 10 l/min.
Es folgt eine detaillierte Verfahrensbeschreibung:
0,2 ml Blut wurden in 10-ml-Kunststoffröhrchen transferiert. Anschließend wurden 0,2 ml 0,5 M Ammoniumcarbonatpuffer (pH 9) hinzugefügt. Eine Flüssig-Flüssig-Extraktion mit 2 ml Ethylacetat wurde 10 Minuten lang ausgeführt. Die Proben wurden 10 Minuten lang bei 4 °C mit 2540 x g zentrifugiert. Die organische Phase wurde in 2-ml-Eppendorf-Röhrchen transferiert und bei 40 °C unter einem Strom von inertem Stickstoffgas bis zur Trocknung evaporiert. Die trockenen Rückstände wurden in 0,05 ml Methanol aufgelöst. Die Lösung wurde dann in Glaseinsätze von Autosampler-Vials transferiert und mittels Ultra-Hochleistungsflüssigkeitschromatographie/Triple-Quadrupol-Tandem-Massenspektrometrie (UHPLC-QqQ-MS/MS) analysiert. Das Injektionsvolumen betrug 2,0 μl. Im Vergleich zu herkömmlichen Methoden verwenden wir nur geringe Mengen an umweltschädlichen organischen Lösungsmitteln und arbeiten mit einem kleinen biologischen Probenvolumen.
Der größte Vorteil dieser Methode besteht darin, dass sie nicht nur schnell und einfach, sondern auch selektiv und empfindlich ist und dank des Einsatzes von UHPLC-MS/MS die zeitgleiche Ermittlung unterschiedlicher PDE-5-Inhibitoren ermöglicht, sodass in forensischen Fällen charakteristische Fragmente in Produktionenspektren bei der Identifizierung solcher Substanzen hilfreich sein können.
Literature/References
- Nichols D.J., Muirhead G.J., Harness J.A. Pharmacokinetics of sildenafil after single oral doses in healthy male subjects: absolute bioavailability, food effects and dose proportionality. Br J Clin Pharmacol. 2002, 53: 5–12.
- Padma-Nathan H. Sildenafil citrate (Viagra) treatment for erectile dysfunction: an updated profile of response and effectiveness. Int J Impot Res 2006, 18(5): 423-31.
- Haczyński J., Gil R. Phosphodiesterase-5 inhibitors therapy in patients treated with nitrates. Seksuologia Polska 2003, 1 (2): 73–78.
- Gresser U., Gleiter C. Erectile dysfunction: Comparison of efficacy and side effects of the PDE-5 inhibitors Sildenafil, Vardenafil and Tadalafil. Review of the literature. Eur J Med Res, 2002, 7: 435–446.
- Turko I.V., Ballard S.A., Francis S.H., Corbi J.D. Inhibition of cyclic GMP-binding cyclic GMP-specific phosphodiesterase (Type 5) by sildenafil and related compounds. Mol Pharmacol 1999; 56: 124–130.
- Huang S.A., Lie J.D. Phosphodiesterase-5 (PDE5) Inhibitors in the Management of Erectile Dysfunction. P T. 2013, 38(7): 414–419.
- Muirhead G.J., Rance D.J., Walker D.K., Wastall P. Comparative human pharmacokinetics and metabolism of single-dose oral and intravenous sildenafil citrate. Br J Clin Pharmacol. 2002, 53(1): 13–20.
- Wang R.C., Jiang F.M., Zheng Q.L., Li C.T., Peng X.Y., He C.Y., Luo J., Liang Z.A. Efficacy and safety of sildenafil treatment in pulmonary arterial hypertension: a systematic review. Respir Med 2014; 108: 531– 537.
- Hatzimouratidis K. Sildenafil in the treatment of erectile dysfunction: an overview of the clinical evidence. Clin Interv Aging. 2006, 1(4): 403–414.
- Pfizer, I. U.S. prescribing information. Viagra: Compound data sheet. 1 (1999).
- Muirhead G.J., Rance D.J., Walker D.K., Wastall P. Comparative human pharmacokinetics and metabolism of single-dose oral and intravenous sildenafil citrate. Br J Clin Pharmacol. 2002, 53(1): 13–20.
- Walker D.K., Ackland M.J., James G.C., Muirhead G.J., Rance D.J., Wastall P., Wright P.A. Pharmacokinetics and metabolism of sildenafil in mouse, rat, rabbit, dog and man. Xenobiotica. 1999, 29(3): 297-310.
- Toni L. De, Rocco Ponce M. De, Franceschinis E., Dall’Acqua S., Padrini R., Realdon N., Garolla A., Foresta C. Sublingual Administration of Sildenafil Oro-dispersible Film: New Profiles of Drug Tolerability and Pharmacokinetics for PDE5 Inhibitors. Front Pharmacol. 2018 6 (9): 59.
- Hyland R., Roe E.G., Jones B.C., Smith D.A. Identification of the cytochrome P450 enzymes involved in the N-demethylation of sildenafil. Br J Clin Pharmacol. 2001, 51: 239–248.
- Jeong C.K., Lee H.Y., Jang M.S., Kim W.B., Lee H.S. Narrowbore high-performance liquid chromatography for the simultaneous determination of sildenafil and its metabolite UK-103,320 in human plasma using column switching. J Chromatogr B Biomed Sci Appl. 2001, 752 (1): 141–147.
- Yeo M., Park Y., Lee H., Choe S., Baek S. H., Kim H. K., Pyo J. S. New metabolites of hongdenafil, homosildenafil and hydroxyhomosildenafil. J Pharm Biomed Anal 2018, 149: 586–590.
- Zou P., Oh S.S.Y., Hou P., Low M.Y., Koh H.L. Simultaneous determination of synthetic phosphodiesterase-5 inhibitors found in a dietary supplement and pre-mixed bulk powders for dietary supplements using high-performance liquid chromatography with diode array detection and liquid chromatography–electrospray ionization tandem mass spectrometry. J Chromatogr A, 2006, 1104(1–2): 113–122.
- Kloner R.A., Zusman R.M. Cardiovascular effects of sildenafil citrate and recommendations for its use. Am J Cardiol. 1999, 84: 11–17.
- Dittrich B., Luger P. Invariom-based comparative electron density studies of iso-sildenafil and sildenafil. Zeitschrift für Naturforschung B, 2017, 72(1): 1–10.
- Choi D.M., Park S., Yoon T.H., Jeong H.K., Pyo J.S., Park J., Kim D., Kwon S.W. Determination of analogs of sildenafil and vardenafil in foods by column liquid chromatography with a photodiode array detector, mass spectrometry, and nuclear magnetic resonance spectrometry. J AOAC Int, 2008, 91(3): 580–588.
- Assemat G., Balayssac S., Gilard V., Martins-Froment N., Fabing I., Rodriguez F., Génisson Y., Martino R., Malet-Martino M. Isolation and identification of ten new sildenafil derivatives in an alleged herbal supplement for sexual enhancement. J Pharm Biomed Anal, 2020, 191: 113482.
- Blok-Tip L., Zomer B., Bakker F., Hartog K.D., Hamzink M., Ten Hove J., Vredenbregt M., de Kaste D. Structure elucidation of sildenafil analogues in herbal products. Food Addit Contam, 2004, 21(8): 737–748.
- Do T.T., Theocharis G., Reich E. Simultaneous detection of three phosphodiesterase type 5 inhibitors and eight of their analogs in lifestyle products and screening for adulterants by high-performance thin-layer chromatography. J AOAC Int, 2015, 98(5): 1226–1233.